2026中考辽宁辽阳市一模 化学试卷及参考答案 智慧化学教学 昌图县杨智超初中化学名师种子工作室 出峡飞舟
- 2026-05-06 10:15:06
关注公众号,再添加微信“Cxfz1972”获取更多化学资源
文章末尾有更多资源链接
2026年初中学业水平考试九年级考试科目模拟考试
化学试卷
(本试卷共14道题 满分50分 化学和物理考试时间共150分钟)
考生注意:所有试题必须在答题卡指定区域作答,在本试卷上作答无效。
可能用到的近似相对原子质量:H—1 C—120—16
第一部分选择题(共10分)
(本部分共包括10道小题,每题1分,每小题只有一个最符合题目要求的选项)
1. 空气的成分中,体积分数约占21%的是
A.氧气B.氮气
C.二氧化碳D.稀有气体
2. 下列符号能表示2个氢原子的是

3. 下列物品由金属材料制成的是
A.不锈钢餐具B.羊毛衫
C.塑料盆D.玻璃杯
4. 荧光粉原料氮化锶(Sr₃N₂)中氮元素的化合价为-3,则锶元素的化合价为
A.-2B.-3
C.+2D.+3
5. 将下列物质放入水中能形成溶液的是
A.食盐B.泥土
C.花生油D.面粉
6. 规范操作对实验成功与安全很重要,下列实验操作正确的是
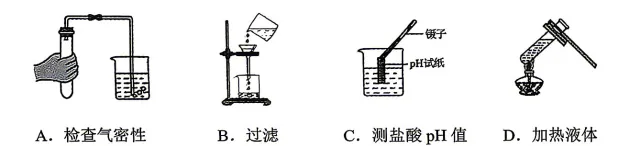
7.“土膏欲动雨频催”,春季为促进作物生长常需施用氮肥。下列物质属于氮肥的是
A.K₂SO₄B.CO(NH₂)2
C.Ca(H₂PO4)2D.KH₂PO₄
8. 一种氯原子的原子核内有17个质子和18个中子,该原子的核电荷数为
A.1 B.17
C.18D.35
9.下列关于物质用途的描述不正确的是
A. 氮气用于食品防腐
B. 熟石灰改良碱性土壤
C. 小苏打是制作面点所用发酵粉的主要成分
D. 稀有气体用于制作电光源
10.电解水实验装置如右图。下列说法不正确的是
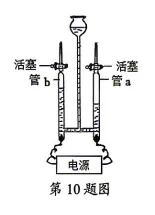
A. b中收集到的气体是氧气
B. a 管连接的电源为正极
C. 水不是一种元素组成的
D. 水在通电的条件下可以生成氢气和氧气
文章末尾有更多资源链接
第二部分 非选择题(共40分)
(本部分共包括4道小题)
11. (10分)实验是学习化学的重要途径。
I.二氧化碳的制备
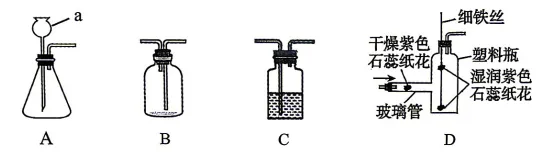
(1)仪 器a 的名称是 。
(2)用大理石和稀盐酸制取CO₂的化学反应方程式为。
(3)若要获得干燥的CO₂ 还需要在A 、B 装置之间增加C 装置,C 中的试剂为 (填名称)。
Ⅱ.二氧化碳的性质验证
将纯净干燥的 CO2缓慢通入装置D, 观察到现象:a.玻璃管内干燥纸花始终未变 色 ;b. 塑料瓶内的下方纸花先变红,上方纸花后变红。
(4)根据上述现象,得出关于CO₂ 的两条性质是、。
(5)将变红的石蕊纸花取出,加热一段时间,纸花重新变成紫色,原因是 ( 用化学方程式表示)。
Ⅲ. 自制蔬菜大棚二氧化碳发生器 【资料】
植物光合作用需要CO₂, CO₂浓度过低光合作用弱,蔬菜生长慢、产量低;CO₂浓度
过高会破坏叶绿体,抑制蔬菜光合作用,影响生长。CO₂浓度监测液判断标准为:
呈蓝色表示CO₂ 量过少;呈绿色表示CO₂ 量正常;呈黄色表示CO₂ 量过多。图1为
蔬菜大棚 中某时段CO₂浓度变化曲线。
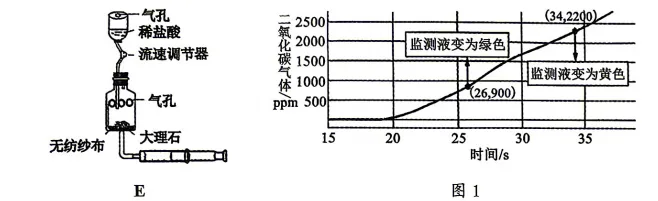
(6) E 装置为小组同学的自制的CO₂发生器,装置中流速调节器与分液漏斗作用类似,可用于,关闭流速调节器后,下方的反应仍在继续,此时可通过操作使反应停止。
(7)在图1中,某时段测得蔬菜大棚内CO₂ 浓度为2200ppm,此时应 (“打开” 或“关闭”)该CO₂ 发生器。
(8)大气中CO₂ 排放过多会造成温室效应加剧,中学生可践行的低碳生活是 。
12. (10分)金属资源的开发与利用贯穿了人类社会发展的全过程。
I.传统工艺
(1)【古法炼金】虽然“点石成金”是神话,但古人通过淘洗金沙获取自然金是现实。 金在自然界中以 (选填“单质”或“化合物”)形式存在,这是由于金的金属活动性 (选填“强”或“弱”)。
(2)【青铜时代】先秦时期,以孔雀石【主要成分为Cu₂(OH)₂CO₃】为原料炼铜,其 受热分解的原理 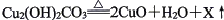 ,其中X 的化学式为 。
,其中X 的化学式为 。
(3)【铁器时代】汉代出现早期炼铁工艺,核心原理与现代高炉炼铁一致,东汉杜诗 发明了“水排”,利用水力驱动鼓风设备向高炉内鼓风,鼓风的目的是。
南北朝灌钢法趋于成熟,利用生铁与熟铁熔炼得到钢,生铁的含碳量比钢 (填“高”或“低”)。
(4)【明清工艺时代】明代《天工开物》中记载,炼锡时需要加入铅使二者混合,从而使合金较易熔化流出,这是因为 。
Ⅱ. 现代工艺
氢冶金技术是以氢气为主要还原剂的新型冶金工艺,其简要工艺流程如下图所示。
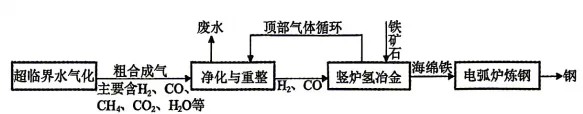
(5)超临界水兼具液体的溶解能力与气体的流动性,是水在高温高压下形成的特殊状态,该过程属于(填“物理”或“化学”)变化。
(6)经过“净化与重整”环节后,CH₄与CO₂在高温、催化剂的条件下生成H₂与 CO输出,写出该反应的化学方程式:。
(7)该流程中引入了“顶部气体循环”,分析循环气体中除了未反应的H₂与CO,还一定含有(答一点)。
(8)相比于传统高炉炼铁,氢冶金技术突出的环保优势在于 (答一点)。
13 . (9分)阅读下面材料。
锂离子电池( LIBs) 凭借高能量密度、长寿命、绿色环保等优势,在新能源汽车、 3C 电子、电化学储能等领域应用广泛。这类电池的正极材料中常含有钴、锂等有价金属, 若大量废旧锂电池不妥善回收,会带来严重的环境与资源浪费问题。
当前废旧锂电池回收主要有火法、湿法和直接回收三类,其中湿法回收是研究与应用的重点。废旧电池经放电、拆解后得到正极材料,与酸溶液和过氧化氢在加热条件下反 应,使金属离子进入浸出液;再经过滤除杂、沉淀等方法实现金属分离与再生利用,其酸浸湿法冶金工艺流程如图1所示。
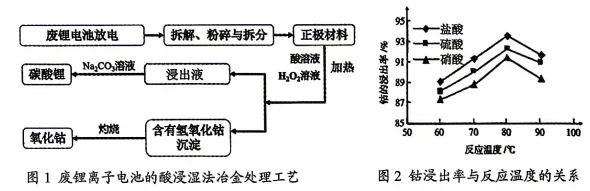
研究人员对比了不同酸—过氧化氢体系在不同温度下的钴浸出率,结果如图2所示。 湿法回收在高效回收金属的同时,需防控酸液泄漏、酸性气体排放等问题。
依据文章内容回答下列问题:
(1)锂离子电池的优点 (答一点)。
(2)图1酸浸湿法冶金中,废旧锂电池回收拆解前先进行,“粉碎”的目的是。
(3)结合图1的沉淀法工艺,含有氢氧化钴[Co(OH)₂]的沉淀是流程中的关键中间产 物,其受热生成氧化钴[CoO]和水,写出该反应的化学方程式,该反应属于(填“分解”或“复分解”)反应。
(4)结合图2曲线,钴浸出率达到最佳时的条件是。在80℃后,钴浸出率明显下降,由此推测H₂O₂具有的一条化学性质。
(5)除了回收并利用废旧金属,保护金属资源的途径还有。
(6)湿法回收工艺在高效回收金属时,还需注意的问题有(答一点)。
14 . (11分)实验小组同学对验证氢氧化钠的性质产生兴趣。
【探究溶解】
(1)向装有NaOH 固体的烧杯中加入少量水溶解,迅速将装有白磷的试管放入所得 溶液中,观察到试管内白磷燃烧,说明NaOH 固体溶解 ,同时也能说明是燃烧的条件之一。(白磷着火点是40℃)
【探究潮解】
(2)同学们对NaOH 固体能在空气中潮解的原因提出以下猜想:
猜想一:NaOH 固体吸收水蒸气而潮解;
猜想二:NaOH 固体与CO₂ 反应生成水使其潮解。
为验证猜想,设计甲实验进行验证,装置如下图甲。
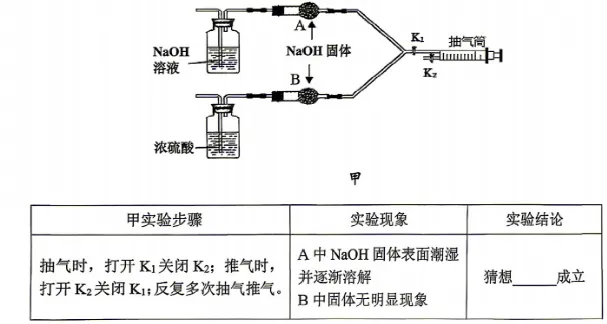
(3)NaOH溶液的作用是吸收,增大的含量,便于观察实验现象。
为了进一步获取证据,进行了乙实验,实验步骤如下:在密闭的三颈烧瓶中(如 图乙,容积为1L) 加入足量的NaOH 固体,用传感器测得瓶内空气中CO₂、水蒸气 含量变化,所得数据如图1所示。
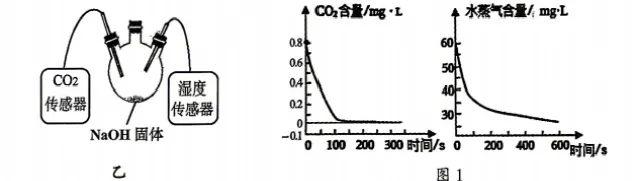
(4)依据图1数据计算,三颈烧瓶中NaOH固体与CO₂反应产生H₂O的质量为 mg (保留一位小数)。
(5)综合计算结果及图1的数据,说明甲实验结论成立的原因:。
【探究变质】
取适量久置后的NaOH 固体于烧杯中,加水溶解,向其中加入足量BaCl2固体(BaCl2溶液显中性,Ba(OH)2可溶于水,BaCO₃不溶于水),并用pH 传感器测反应前后酸碱度变化如图2所示。
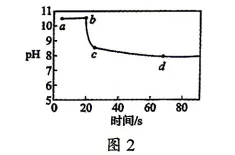
(6)bc段下降的要原因:(用化学方程式表示)。
(7)由图2可知该样品中NaOH固体(选填“部分变质”或“完全变质”)。
(8)本实验加入的是BaCl₂固体,不选择BaCl₂溶液的原因是。
(9)结合上述探究,提出保存NaOH固体的合理建议:(答一点)。

供稿:出峡飞舟
审核:昌图县杨智超初中化学名师种子工作室
版权:资料来源于网络,如商用转载,请先关注公众号,再添加公众号管理员“Cxfz1972”微信号!
如若您喜欢该篇文章敬请转发、分享!
九年级化学精品课七十二 走进化学世界 4大考点15大题型 智慧化学教学 昌图县杨智超初中化学名师种子工作室
2026年中考一模 沈阳市于洪区 化学试卷及参考答案 昌图县杨智超初中化学名师种子工作室 智慧化学教学
义务教育之殇——(七)恪尽职守、以兴教化 昌图县杨智超初中化学名师种子工作室 出峡飞舟 智慧化学教学
2026中考一模沈阳市大东区九年级化学试卷及参考答案 昌图县杨智超初中化学名师种子工作室 智慧化学教学
九年级化学精品课 七十一 《空气和氧气》单元学情调研试卷及参考答案 昌图县杨智超初中化学名师种子工作室 智慧化学教学 出峡飞舟
2026年中考一模沈阳市浑南区 昌图县杨智超初中化学名师种子工作室 智慧化学教学 出峡飞舟

辽阳白塔
