第二部分化学
★可能用到的相对原子质量:H-1C-12N-14O-16Na-23P-31Cl-35.5Ca-40
一、选择题(共13题,共18分。24~31题,每题1分;32~36题,每题2分。在每题给出的四个选项中,只有一项符合题目要求)
钙是人体骨骼和牙齿的重要成分,主要以羟基磷酸钙[Ca10(PO4)6(OH)2]的形式存在。钙在元素周期表中的信息及原子结构示意图如图。回答24~26题:
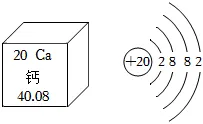
24.下列关于人体健康的说法错误的是( )
A.钙是人体必需的微量元素B.合理膳食结构,保证营养均衡
C.青少年长期缺钙易患佝偻病D.长期饮用碳酸饮料会腐蚀牙齿
25.下列关于钙元素或钙原子的说法错误的是( )
A.元素符号为CaB.原子核外共有4个电子层
C.核电荷数为20D.易失去2个电子,形成Ca2-
26.下列关于羟基磷酸钙[Ca10(PO4)6(OH)2]的说法正确的是( )
A.含有两种金属元素B.钙元素的化合价为0
C.氢元素的质量分数最小D.磷、氧原子的个数比为1:4
27.在“测定土壤酸碱性”实验中,下列操作错误的是( )
28.某兴趣小组为学校美育节带来了不同书法作品。下列说法正确的是( )
A.图A是用碳素墨水在白纸上书写的“大”字,该墨水中石墨的化学式为C60
B.图B是用浓硫酸在白纸上写出黑色的“美”字,其利用了浓硫酸的吸水性
C.图C是用硫酸铜溶液在铁片上书写后变红的“湖”字,该反应属于置换反应
D.图D是先用酚酞溶液在白纸上写出“北”字,再盖在碳酸饮料上方,颜色由紫变红
29.二十四节气蕴含丰富的文化内涵,反映了我国劳动人民的智慧。下列说法错误的是
( )
A.清明:草木萌发,绿色植物通过光合作用释放氧气
B.小满:农作物的颗粒逐渐饱满时,农业上需合理使用化肥
C.大暑:炎热天气能加快食物发生化学变化而变质
D.冬至:传统习俗腌制腊肉、制作泡菜可以使用工业用盐
30.2026春晚舞台上的武打机器人采用钛铝合金作为骨架材料,石墨烯作为电子皮肤。下列说法错误的是( )
A.铝合金的熔点高于纯铝,适合在高温环境工作
B.钛铝合金属于混合物,其硬度大于纯钛或纯铝
C.机器人骨架表面形成的致密氧化膜能有效防止金属腐蚀
D.石墨烯是一种由碳原子构成的单层片状结构的新材料,属于无机非金属材料
31.海洋是地球上最大的储水库,还可提供重要的清洁能源。我国科学家将海水淡化与利用太阳能光伏发电电解水结合起来,实现了海水的高效制氢(装置如图,聚四氟乙烯薄膜只允许水分子通过)。下列说法错误的是( )
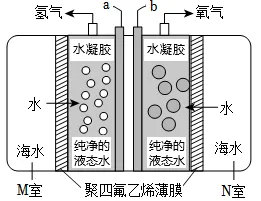
A.导线a端接电源的负极
B.聚四氟乙烯薄膜与活性炭原理相同
C.电解时,M、N室中海水含盐的浓度均增大
D.太阳能使用成本低,属于可再生能源
32.“千锤万凿出深山,烈火焚烧若等闲。粉骨碎身浑不怕,要留清白在人间”。这是明代民族英雄于谦的传世佳作,蕴含着丰富的化学知识。诗中描绘的烧制熟石灰及其应用过程如图。下列说法正确的是( )

A.②发生反应后质量减轻,违背质量守恒定律
B.③发生反应时放出热量
C.④发生反应的化学方程式是CaO + CO2 ═ CaCO3
D.石灰石、生石灰、熟石灰三种物质含有相同的元素种类
33.教材中的“方法导引”为化学学习提供了基本思路和方法,下列所举示例正确的是( )
A.模型:现在科学研究表明道尔顿原子模型是正确的
B.分类:化合物可分为酸、碱、盐、氧化物,纯碱属于碱
C.定量认识:31g红磷在31g氧气中充分燃烧,生成62g五氧化二磷
D.分析解释:稀盐酸和稀硫酸都能与碱反应,是因为酸溶液里都含有氢离子
34.我国科学家在“人工固氮”领域取得重要突破,成功研制出一种新型催化剂,可将氮气和水转化为氨气并释放氧气,该反应的微观示意图如图。下列说法正确的是( )
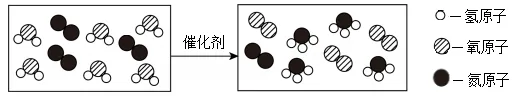
A.该反应涉及两种氧化物B.参加反应的氮气与水的分子个数比为1:2
C.生成氨气和氧气质量比为17:24D.化学反应前后,催化剂的质量和性质不变
35.室温下,向一定体积10%的氢氧化钠溶液中滴加10%的稀盐酸,测得溶液温度变化与加入盐酸体积的关系如图(Δt为溶液实时温度与初始温度差),下列说法错误的是( )
A.滴加盐酸的全过程中,氯化钠的溶解度先增大后减小
B.滴加盐酸的体积为14mL时,所得溶液的pH<7
C.该反应的微观实质是H+ + OH﹣= H2O
D.二者恰好完全反应时,消耗的稀盐酸与氢氧化钠溶液的质量相等
36.某学习小组设计的下列实验方案,能达到目的的是( )
A.配制100g溶质质量分数为10%的NaCl溶液
B.探究水是铁生锈的必要条件
C.验证金属活动性顺序为Fe>Cu>Ag
D.能说明NaOH溶液与CO2发生反应
二、非选择题(共7题,共32分)
37.(4分)甲骨、简牍、丝帛、芯片作为文字载体,在中华文明传承过程中发挥重要作用。

(1)如图1用青铜刀在甲骨上刻字,属于_________(填“物理”或“化学”)变化。
(2)如图2竹简在加工过程中要进行蒸煮、晾晒,防霉等。晾晒能晒干水分的微观原因是___________________________。
(3)图3纸书《天工开物》有锻造铁器的记载,“受锻之时,十耗其三为铁华、铁落”。“铁华、铁落”中含有四氧化三铁,写出生成该物质的化学方程式_____________。
(4)图4芯片是如今文字记录载体,它的主要成分是硅。制备粗硅的化学方程式为SiO2 + 2C Si + 2X↑,则X的化学式是___________。
Si + 2X↑,则X的化学式是___________。
38.(4分)阅读科普短文,回答下列问题。
纳米海绵是一种新型环保清洁产品,具有网状多孔结构,有良好的吸油能力、对环境友好等特性,清洁过程中可以吸附物体表面污渍,可用于清洁茶垢、油垢等,还可解决海上石油泄漏造成的污染。科学家测定纳米海绵对不同油品的吸油能力(吸油质量比越高,其吸油能力越强),结果如图1。吸油能力的差异性取决于油品自身的密度,油品密度越大,纳米海绵的吸油能力越强。
纳米海绵还具有良好的循环利用性。通过挤压,可将纳米海绵吸附的油品挤出,经洗涤干燥后再次使用,两种吸油材料对泵油的循环吸收测试结果如图2。
(1)纳米海绵具有等特性(写1点)。
(2)由图1可知纳米海绵对(填油品名称)的吸收能力最强。
(3)由图2可得到的实验结论:在其他条件相同时,,纳米海
绵吸油能力变化不明显,细菌纤维素的吸油能力变弱。
(4)纳米海绵是以三聚氰胺和甲醛(HCHO)为原料制得的高分子物质。已知甲醛在空气中充分燃烧生成二氧化碳和水,该反应的化学方程式为。
39.(5分)硝酸铜可用于陶瓷着色、也可用于制备波尔多液。利用含铜废料(含Cu、CuS)制备Cu(NO3)2 • 3H2O晶体的流程如图。
资料1:硝酸(HNO3)受热易分解,且具有挥发性
资料2:降温结晶时,若降温太快,会导致晶体细碎,无法得到较大颗粒的晶体
(1)“焙烧”:CuS转化为SO2和一种黑色固体,则该黑色固体的化学式为。
(2)“酸化”:溶液变为蓝色,发生反应的化学方程式是_______________________。
(3)“置换”:需要在通风环境中进行反应的原因是___________________________。
(4)“转化”:实验室在图1的装置中完成“转化”过程。该过程利用流水冷却,控制温度在55℃左右,温度不宜过高的原因是______________________________。
(5)从转化所得溶液中获得较大颗粒Cu(NO3)2▪3H2O晶体的方法是:蒸发浓缩、降温结晶、过滤、洗涤、干燥。结合信息和图2分析,降温结晶时需要控制的条件是_________。
40.(5分)2025年11月包信和院士团队在天然气转化乙烯(C2H4)领域取得了世界级的突破,基本原理可表示为2CH4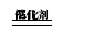 C2H4 + 2H2。请计算:
C2H4 + 2H2。请计算:
(1)乙烯(C2H4)中碳、氢元素的最简质量比为。
(2)若要制得14t乙烯,至少需要甲烷的质量是多少t(写出计算过程)?
41.(4分)某化学兴趣小组的同学利用下图所示的装置来制取和检验气体,请回答:
(1)仪器m的名称是。
(2)用装置B、C制取氧气,装置B内液体液面应加到(填“a”或“b”)处。用装置D收集氧气,将带火星的木条平放在瓶口,若观察到,则说明氧气已集满。
(3)用装置E除去CO2中混有的少量HCl气体,发生反应的化学方程式是。
42.(6分)化冰盐是常用的融雪剂,主要用于城市道路积雪处理以保证人们出行安全。某项目式学习小组对化冰盐融雪原理、成分及对环境的影响产生兴趣并展开探究。
任务一:了解化冰盐融雪原理。该小组经走访了解,本地使用的某种化冰盐含NaCl,
可能含MgCl2、MgSO4、CuSO4中的一种或多种。
(1)撒化冰盐融雪的原理是_______(填“升高”或“降低”)混合物的凝固点,从而防止雪水结冰。
任务二:探究化冰盐成分。该小组为探究该化冰盐成分,设计并完成以下实验。
(2)操作a的名称是_______。
(3)加入足量NaOH溶液,一定发生的化学方程式是_________________________。
(4)依实验信息,该化冰盐中无法确定的物质是__________(写名称)。
任务三:调查化冰盐对环境的影响。常见化冰盐的危害如下表:
| 氯化钠 | 氯化镁 | 硫酸镁 | 醋酸钙镁 |
对金属的腐蚀 | 100% | 120%~150% | 40%~60% | ≤5% |
对水泥的腐蚀 | 100% | 110%~130% | 50%~70% | ≤10% |
对地下水影响 | 100% | 150%~200% | 70%~90% | 80% |
对土壤的影响 | 导致土壤板结 | 影响较小 | 导致土壤酸化 | 几乎无影响 |
【反思评价】
(5)由上表可知,使用硫酸镁作化盐时,若要降低对土壤的影响,可采取的措施是________________。
(6)你对道路除雪提出的建议有______________________(写1点)。
43.(4分)我国研究团队提出基于绿氢和生物质富氧燃烧技术“零碳甲醇(CH3OH)合成系统”,基本组成如图1。甲醇可通过二氧化碳加氢合成,合成过程中其产率随温度变化的关系如图2。甲醇完全燃烧生成二氧化碳和水。
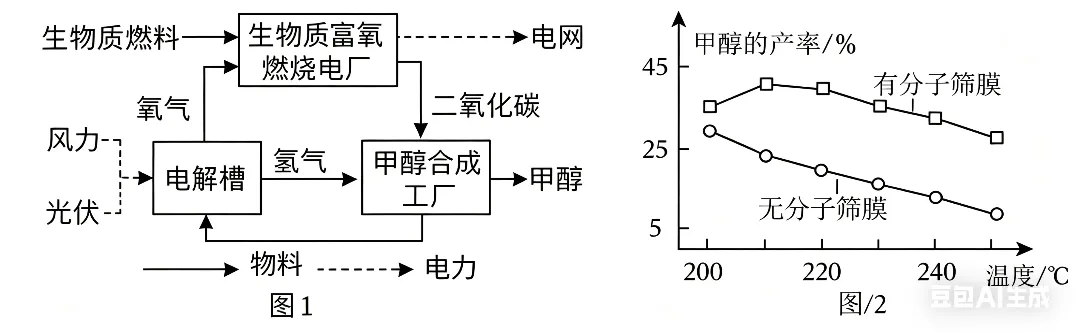

(1)图1“电解槽”中,理论上产生氢气和氧气的分子个数比为。
(2)图1“甲醇合成工厂”中,在一定条件下发生反应的化学方程式为。
(3)由图2可知,合成甲醇应选择的最佳条件为。
(4)甲醇被称为“零碳”燃料,更准确的说是“零增碳”的原因是 。
2026年九年级四月教学调研考试
化学试卷参考答案与评分说明
说明:有关化学方程式书写的评分标准:化学式书写正确,其他错误给0.5分。书写完全正确给1分
一、选择题(共13个题,共18分。24~31题中每题1分;32~36题中每题2分。在每题给出的四个选项中,只有一项符合题目要求)
题号 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 | 35 | 36 |
答案 | A | D | C | B | C | D | A | B | B | D | C | D | C |
二、非选择题(共7个题,共32分)
37. (1)物理
(2)温度升高,分子运动速率加快
(3)3Fe + 2O2Fe3O4(条件写高温也可)
(4)CO
38. (1)良好的吸油能力(或对环境友好或良好的循环利用性)
(2)四氯化碳
(3)循环使用次数1~8之间,随循环使用次数的增加
(4)HCHO + O2CO2+ H2O
39. (1)CuO
(2)CuO + H2SO4= CuSO4+ H2O
(3)有可燃气体氢气产生,防止发生爆炸
(4)防止HNO3、H2O2分解,提高原料利用率
(5)保持温度在26.4℃以上缓慢降温结晶
40.(1)6∶1………………………………………………………1分
(2)解:设至少需要甲烷的质量为x ………………………………0.5分
2CH4C2H4+ 2H2
32 28
x14t …………………………1分
= …………………………1分
x=16t ……………………………………1分
答:至少需要甲烷的质量为16t。 ………………………………0.5分
(其它合理解法均给分)
41.(1)试管
(2)a 带火星小木条复燃(或复燃)
(3)NaHCO3+ HCl = NaCl + H2O + CO2↑
42.(1)降低
(2)过滤
(3)MgSO4+ 2NaOH = Mg(OH)2↓+ Na2SO4
(4)氯化镁
(5)与碱性物质混合使用(合理均可)
(6)减少化冰盐使用(或用危害小的化冰盐如醋酸钙镁、机械除雪与化冰盐结合等)
43.(1)2∶1
(2)CO2+ 3H2 一定条件CH3OH + H2O
(3)有分子筛膜、210℃
(4)生产甲醇消耗的CO2与燃烧等量的甲醇生成的CO2质量相等
总第123期